Διαφορά μεταξύ μεταλλικών και μη μεταλλικών στοιχείων
Μέταλλα και μη μεταλλικά
Και τα μέταλλα και τα μη μεταλλικά μπορούν να αποτελούν μέρος του περιοδικού πίνακα, αλλά υπάρχουν πολλές διαφορές μεταξύ του μετάλλου και των μη μεταλλικών χημική και φυσική σύνθεση. Τα περισσότερα στοιχεία του περιοδικού πίνακα είναι μέταλλα και μόνο λίγα είναι μη μεταλλικά. Αυτά τα στοιχεία είναι διατεταγμένα στον πίνακα από την ηλεκτρονική δομή τους. Είναι πάντα χρήσιμο να μάθετε τη διαφορά μεταξύ των δύο προκειμένου να τα καταλάβετε με μεγαλύτερη σαφήνεια.
Τι είναι τα μέταλλα;
Τα μέταλλα είναι καλοί οδηγοί ηλεκτρικής ενέργειας. Είναι λαμπερά και ευέλικτα. Τα περισσότερα μέταλλα μπορούν να χυθούν σε λεπτά φύλλα ή να στραγγιστούν για να γίνουν λεπτά σύρματα. Τα μέταλλα τείνουν να χάνουν ηλεκτρόνια όταν υποβάλλονται σε χημικές αλλαγές. Τα μέταλλα μπορούν επίσης να είναι ένας καλός αναγωγικός παράγοντας. Ο υδράργυρος είναι το μόνο μέταλλο που είναι υγρό σε θερμοκρασία δωματίου, τα περισσότερα μέταλλα είναι διαφορετικά στερεά.
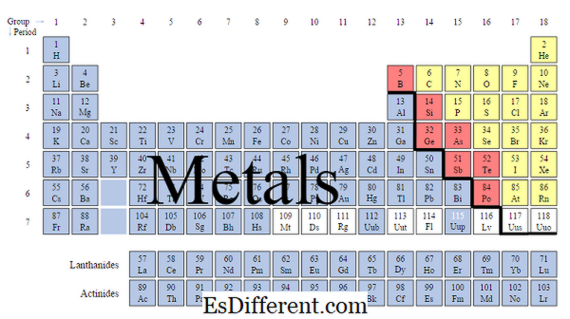
Τι είναι τα μη μεταλλικά στοιχεία;
Τα μη μεταλλικά, από την άλλη πλευρά, ποικίλουν σε σχήματα και μεγέθη. Έρχονται επίσης σε διαφορετικά χρώματα. Είναι εύθραυστα και μπορούν να είναι σκληρά και μαλακά. Τα μη μεταλλικά προϊόντα δεν έχουν την ικανότητα να εκτελούν ηλεκτρική ενέργεια καλά. Είναι καλοί οξειδωτικοί παράγοντες και μπορεί να είναι υγρό, στερεό ή αέριο σε θερμοκρασία δωματίου. Όταν τα μέταλλα συνδυάζονται ή αντιδρούν με ένα μη μεταλλικό, τα μη μεταλλικά αποκτούν ηλεκτρόνια καθιστώντας έτσι ανιόντα.
Ποια είναι η διαφορά μεταξύ Metals και Nonmetals;
Και τα μέταλλα και τα μη μέταλλα έχουν διαφορές τόσο στις χημικές όσο και στις φυσικές ιδιότητες.
Τα μέταλλα είναι μεγάλοι αγωγοί ηλεκτρισμού και θερμότητας και όταν υποβάλλονται σε χημικές αλλαγές χάνουν ηλεκτρόνια και γίνονται κατιόντα. Επίσης, τα μέταλλα είναι στερεά σε θερμοκρασία δωματίου και είναι εύκαμπτα και τεντώσιμα. Συνήθως, έχουν ένα ή δύο χρώματα που είναι ως επί το πλείστον ασήμι σε σκιά.
Τα μη μέταλλα, από την άλλη πλευρά, δεν είναι αγωγοί τέτοιων και κερδίζουν ηλεκτρόνια και μετατρέπονται σε ανιόντα όταν υποστούν χημικές μεταβολές. Επίσης, τα μη μέταλλα μπορούν να είναι είτε στερεά, είτε υγρά είτε αέρια και να διατίθενται σε διάφορα χρώματα. Είναι εύθραυστα και μη τεντώσιμα ή άκαμπτα αν είναι σε στερεά μορφή τους.
->Παραπομπή εικόνας: Periodic_table. svg: Από το παράγωγο έργο του Cepheus: TheSmuel (Periodic_table. svg) [Δημόσιος τομέας], μέσα από το Wikimedia Commons



