Διαφορά μεταξύ αλκαλικότητας και βασικότητας | Αλκαλικότητα Vs Βασικότητα
- Αλκαλικότητα έναντι βασικότητας
Οι δύο όροι "αλκαλικότητα" και "βασικότητα" είναι αρκετά συγκεχυμένοι. Οι περισσότεροι άνθρωποι γνωρίζουν ότι υπάρχει μια διαφορά μεταξύ αυτών των δύο παραμέτρων, αλλά μόνο μερικές από αυτές είναι σε θέση να το ορίσουν σωστά. Η διαφορά κλειδιού μεταξύ αυτών των δύο όρων εξηγείται καλύτερα στους ορισμούς τους. Η βασικότητα είναι ένα μέτρο που εξαρτάται άμεσα από την αλκαλικότητα της κλίμακας pH και , πόση οξύ χρειάζεται για να μειώσει το pH σε μια σημαντική τιμή οξύτητας . είναι επίσης γνωστή ως η ικανότητα αποθήκευσης ενός υδατικού συστήματος . Με άλλα λόγια, η τιμή pH των βασικών διαλυμάτων κυμαίνεται από 7-14. όπου οι λύσεις με υψηλές τιμές pH είναι πιο βασικές. Και οι δύο έχουν ορισμένους ορισμούς, αλλά η γενική ιδέα είναι παρόμοια.
Τι είναι η Αλκαλικότητα;
Η αλκαλικότητα είναι μία από τις σημαντικότερες παραμέτρους στα υδρόβια σώματα και είναι πολύ σημαντική για τους υδρόβιους οργανισμούς . Η αλκαλικότητα μετρά την ικανότητα των υδατικών συστημάτων να εξουδετερώνουν τα οξέα και τις βάσεις. Με άλλα λόγια, η ρυθμιστική ικανότητα ενός υδάτινου σώματος είναι να διατηρεί την τιμή του pH σε μια αρκετά σταθερή τιμή. Το νερό που περιέχει διττανθρακικά (HCO 3 - ), ανθρακικά άλατα (CO 3 2-. μπορούν να συνδυαστούν με ιόντα Η + σε νερό για να αυξήσουν το pH (γίνεται πιο βασικό) του νερού. Όταν η αλκαλικότητα είναι πολύ χαμηλή (η ικανότητα αποθήκευσης είναι χαμηλή), οποιοδήποτε οξύ που προστίθεται στο υδατικό σώμα μειώνει το pH του σε υψηλότερη όξινη τιμή.
- . Στη θεωρία Bronsted-Lowry, οι δέκτες πρωτονίων καλούνται βάσεις. Σύμφωνα με τη θεωρία Lewis, ένας δότης ηλεκτρονίων ζεύγους ονομάζεται βάση. Η βασικότητα είναι ο ιονισμός της αντοχής για την παραγωγή ιόντων OH - , η ικανότητα να δέχονται πρωτόνια ή την ικανότητα να δωρίζουν ηλεκτρόνια.

Αλκαλικότητα:
Πολλοί ορισμοί υπάρχουν.
Η αλκαλικότητα είναι η ικανότητα εξουδετέρωσης οξέων διαλυμένων ουσιών σε δείγμα νερού που μετράται σε χιλιοστοϊσοδύναμα ανά λίτρο.
Το άθροισμα των τιτλοδοτούμενων ανθρακικών και μη ανθρακικών χημικών ειδών σε δείγμα φιλτραρισμένου νερού. Η ικανότητα του νερού να εξουδετερώνει ένα όξινο διάλυμα.
Η ικανότητα ρύθμισης του νερού για να διατηρεί ένα αρκετά σταθερό pH, χωρίς να μεταβάλλει την τιμή του pH, όταν προστίθεται οξύ.
Βασικότητα:
Χρησιμοποιούνται τρεις θεωρίες για τον ορισμό της οξύτητας και της βασικότητας.
Arrenhius:
Βάσεις είναι τα είδη που ιονίζουν για να παράγουν OH -
στο νερό. Η βασικότητα αυξάνεται καθώς ιονίζουμε περισσότερο, δίδοντας OH - σε νερό. Αποδέκτες Proton (H + ) Bronsted-Lowry:
ονομάζονται βάσεις. Lewis: Οι δότες ηλεκτρονίων ζευγών καλούνται βάσεις. Παράγοντες που επηρεάζουν την αλκαλικότητα και τη βασικότητα:
Αλκαλικότητα: Η αλκαλικότητα δεν εξαρτάται από την τιμή του pH. τα υδάτινα σώματα μπορούν να έχουν είτε χαμηλότερη τιμή (πολύ όξινη) είτε υψηλότερη (βασική) τιμή pH με υψηλότερη τιμή αλκαλικότητας. Η αλκαλικότητα καθορίζεται από διάφορους παράγοντες, όπως τα πετρώματα, το έδαφος, τα άλατα και ορισμένες βιομηχανικές δραστηριότητες
(τα λύματα που περιέχουν σαπούνι και απορρυπαντικά είναι αλκαλικά) από τον άνθρωπο. Για παράδειγμα, οι περιοχές όπου υπάρχει ασβεστόλιθος (CaCO
3 ) είναι σημαντικά διαθέσιμες μπορεί να έχουν περισσότερο αλκαλικό νερό. Βασικότητα: Οι παράγοντες που επηρεάζουν την βασικότητα μιας ένωσης ποικίλλουν ανάλογα με τον ορισμό της βασικότητας. Για παράδειγμα, η διαθεσιμότητα ζεύγους ηλεκτρονίων μιας βάσης εξαρτάται από τρεις παράγοντες. Ηλεκτρονική δραστικότητα : CH3-> NH2-> HO-> F-
Όταν εξετάζουμε τα άτομα στην ίδια σειρά στον περιοδικό πίνακα, το πιο ηλεκτροαρνητικό άτομο έχει την υψηλότερη βασικότητα. Μέγεθος
: F-> Cl-> Br-> I- Όταν εξετάζουμε μια σειρά από τον περιοδικό πίνακα, όσο μεγαλύτερο είναι το ηλεκτρόνιο, τόσο μικρότερη είναι η πυκνότητα ηλεκτρονίων.
Resonance
: RO-> RCO 2-
Τα μόρια που έχουν περισσότερες δομές συντονισμού είναι λιγότερο βασικά, καθώς η λιγότερη διαθεσιμότητα ηλεκτρονίων από ένα εντοπισμένο αρνητικό φορτίο.
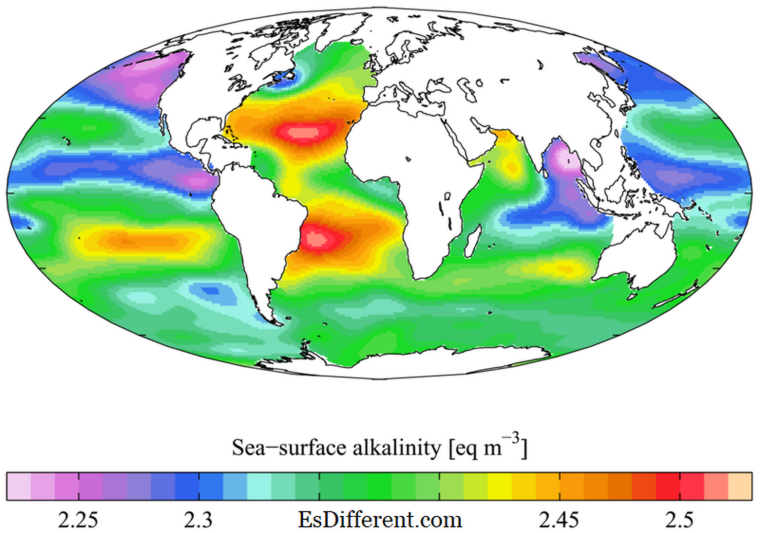
Ευγένεια εικόνας: 1. "WOA05 GLODAP pd ALK AYool" από Plumbago - δική δουλειά. [CC BY-SA 3. 0] μέσω Commons 2. "Thomas Martin Lowry2" από τον Ανώνυμο - Νεκρολογία από το Faraday Soc. (1936). [Δημόσιος τομέας] μέσω Commons


